Прежде чем углубиться в концепцию персонализированной онкологии, необходимо кратко рассмотреть общее представление о персонализированной медицине. На протяжение многих лет предпринимались многочисленные попытки сформулировать исчерпывающее определение точной и персонализированной медицины («personalized medicine»), однако к настоящему моменту единого и всеобъемлющего определения так и не было достигнуто.
Важно отметить, что персонализированный подход не является новшеством последних лет. Исторически медицина, включая онкологическую практику, всегда стремилась быть ориентированной на пациента, предлагая оптимальные решения на основе достижения науки и технологий в определенный период времени. Однако разнообразие факторов, которые формируют концепцию персонализации медицинских решений, изменяется вместе с эволюцией медицины. Развитие клинической генетики и молекулярной онкологии задают новый облик персонализированной медицины и онкологии в наши дни.
К примеру, по данным PubMed, до марта 2024 года было опубликовано 115 464 статьи с упоминанием термина «персонализированная медицина», из которых 90% вышли в свет после 2010 года. Этот факт свидетельствует о том, что внимание к понятию «персонализированной медицины» значительно возросло в последние два десятилетия. Такой интерес к данной концепции напрямую связан с новыми открытиями в области молекулярно-генетических особенностей заболеваний, а также с повсеместным использованием инструментов, позволяющих на основе разнообразных молекулярных данных и клинических характеристик пациента предложить оптимальный терапевтический подход.
Эта идея хорошо отражена в описании консультативной группы ЕС «Горизонт 2020», которая характеризует концепцию точной медицины как «использование индивидуальных фенотипов и генотипов (например, молекулярное профилирование, медицинская визуализация и данные о стиле жизни) для адаптации правильной терапевтической стратегии для конкретного человека в нужное время и/или для определения предрасположенности к заболеванию, а также для обеспечения своевременной и целенаправленной профилактики».
Masucci M, Karlsson C, Blomqvist L, Ernberg I. Bridging the Divide: A Review on the Implementation of Personalized Cancer Medicine. J Pers Med. 2024 May 24;14(6):561. doi: 10.3390/jpm14060561.
Nimmesgern E, Benediktsson I, Norstedt I. Personalized Medicine in Europe. Clin Transl Sci. 2017 Mar;10(2):61-63. doi: 10.1111/cts.12446.
Онкология стала основным направлением, где принципы персонализированной медицины получили свое развитие.
Открытие специфических молекулярных характеристик опухолей позволило задумать нацеленные (таргетные) на такие мишени лекарственные препараты. То есть появилась реальная физическая возможность управлять болезнью в зависимости от молекулярных сведений конкретной опухоли. В начале 2000-х были внедрены в клиническую практику таргетные препараты (таргет или target - в переводе мишень), которые уже стали привычными в практике врача-онколога. Они основаны на принципе “ключ-замок”: обнаружена мишень к препарату - можем назначать лекарственное средство. Примером служит широко известный трастузумаб (анти- HER2 препарат) (рис 1).
Рисунок. 1 Мишень HER2 и препарат трастузумаб на поверхности опухолевых клеток/
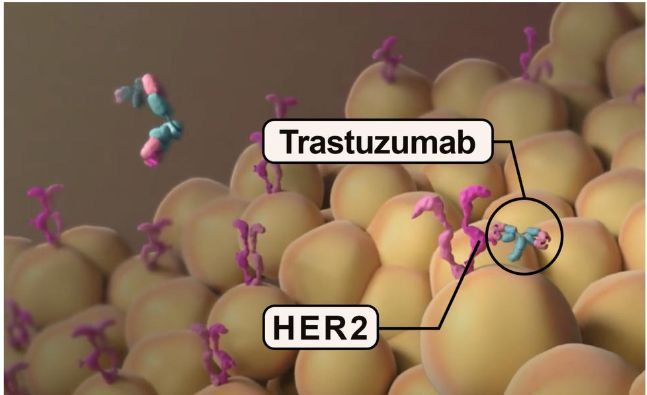
Источник изображения: сайт Национального института рака США https://www.cancer.gov/news-events/cancer-currents-blog/2020/endometrial-cancer-usc-her2-trastuzumab
Наряду с биомаркерами, свидетельствующими о наличии мишени для препарата появилось множество других, которые могут говорить о неэффективности определенных лекарств для конкретной опухоли (резистентности заболевания к определенным типам лечения), помогают уточнить диагноз, характеризуют отдельные подгруппы заболевания, дают сведения об ожидаемом прогнозе и др.
Иммунотерапия
Параллельно развивалось понимание молекулярных механизмов уклонения опухолей от иммунологического надзора. В 2018 году лауреатами Нобелевской премии стали Джеймс Эллисон и Тасуку Хондзё за открытие иммунотерапии злокачественных новообразований. Они показали особый механизм, благодаря которым опухоль “выключала” иммунные Т-клетки из процесса распознавания “врага”, а также предложили как можно этот процесс предотвратить. Сегодня широко известно взаимодействие опухоли и T-лимфоцитов через PD-L1\ PD-1 молекулы. С этим связаны и молекулярные иммуногистохимические тесты на наличие в опухоли PD-L1 и препараты анти-PD-1 (пембролизумаб, ниволумаб) и анти-PD-L1 (атезолизумаб, авелумаб, дурвалумаб).
Рисунок 2. Взаимодействие опухоли и Т-лимфоцита, точки приложения для иммунных препаратов.
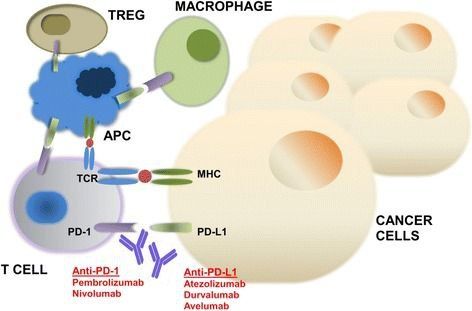
Источник изображения: Gong J, Chehrazi-Raffle A, Reddi S, Salgia R. Development of PD-1 and PD-L1 inhibitors as a form of cancer immunotherapy: a comprehensive review of registration trials and future considerations. J Immunother Cancer. 2018 Jan 23;6(1):8. doi: 10.1186/s40425-018-0316-z.
Иммунотерапия ингибиторами PD-1, PD-L1, CTLA4 и др. точки вошла в рутинную клиническую практику и одобрена к использованию.
Текущие алгоритмы принятия решения по лечению немелкоклеточного рака легкого от Европейского общества медицинских онкологов (ESMO) могут служить наглядной демонстрацией эволюции знаний врачей-онкологов о молекулярно-генетических особенностях отдельных онкологических нозологий (рис 3):
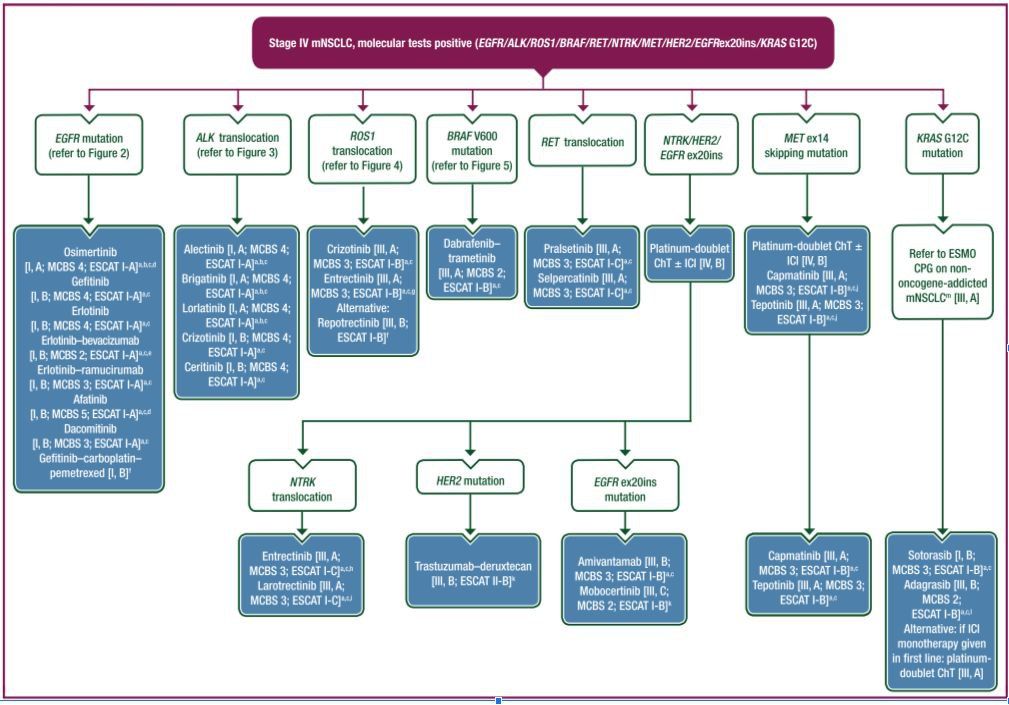
Источник изображения: Hendriks LE, Kerr KM, Menis J, Mok TS, Nestle U, Passaro A, Peters S, Planchard D, Smit EF, Solomon BJ, Veronesi G, Reck M; ESMO Guidelines Committee Oncogene-addicted metastatic non-small-cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023 Apr;34(4):339-357. doi: 10.1016/j.annonc.2022.12.009.
Противоопухолевые лечебные вакцины - активно исследуемые сегодня иммунотерапевтические средства.
Это разрабатываемый исследователями иммунотерапевтический подход к лечению различных злокачественных опухолей. В ряде стран есть противоопухолевые вакцины, одобренные для клинического использования (США, Япония, Китай, Канада, ЕС, Австралия). Например, Sipuleucel-T (PROVENGE, Dendreon), аутологичная клеточная иммунотерапия, изготовленная из антигенпрезентирующих клеток (иммунные дендритные клетки), подготовленных для распознавания простатической кислой фосфатазы. Sipuleucel-T был первым иммунотерапевтическим продуктом, одобренным FDA США в 2010 году для лечения рака предстательной железы. Также широко известна вакцина для лечения меланомы на основе онколитического вируса (генетически модифицированном вирусе простого герпеса) Talimogene Laherparepvec (T-VEC), одобренная к клиническому использованию в США с 2015 г.
Однако все еще предстоит преодолеть ряд препятствий перед тем, как некоторые из решений для отдельных нозологий станут частью регулярной клинической онкологической практики. В России пока не одобренных к клиническому использованию вакцин, активно идут исследования.
Подробно про вакцины, классификации, механизм действия, текущие одобрения и активные КИ рассмотрим в отдельной статье.
Kaczmarek M, Poznańska J, Fechner F, Michalska N, Paszkowska S, Napierała A, Mackiewicz A. Cancer Vaccine Therapeutics: Limitations and Effectiveness-A Literature Review. Cells. 2023 Aug 28;12(17):2159. doi: 10.3390/cells12172159.
Cheever MA, Higano CS. PROVENGE (Sipuleucel-T) in prostate cancer: the first FDA-approved therapeutic cancer vaccine. Clin Cancer Res. 2011 Jun 1;17(11):3520-6. doi: 10.1158/1078-0432.CCR-10-3126.
Handy CE, Antonarakis ES. Sipuleucel-T for the treatment of prostate cancer: novel insights and future directions. Future Oncol. 2018 Apr;14(10):907-917. doi: 10.2217/fon-2017-0531.
Эволюция решений персонализированной онкологии в различных нозологиях крайне неоднородна.
К сожалению, далеко не для всех заболеваний нашлись те самые решения персонализированной онкологии, которые коренным образом поменяли алгоритмы принятия клинических решений. Еще предстоит открыть новые молекулярные биомаркер, разработать новые препараты. Однако есть важное достижение, которое подарил нам “биомаркер-ориентированный подход” при выборе лекарственного противоопухолевого средства - это возможность взглянуть на онкологическое заболевание вне зависимости от его тканевого происхождения (“опухоль-агностически”), посмотреть на совокупность молекулярно-генетических черт, учесть опыт лечения в других онкологических нозологиях, результаты исследований в данной области и всё-же попытаться предложить индивидуальное решение за пределами стандартов, а также найти лучшее клиническое исследование для пациента.
Комплексное геномное профилирование опухоли методом высокопроизводительного секвенирования следующего поколения как инструмент расширенного молекулярно-генетического тестирования опухоли.
Чтобы полноценно охватить известные на сегодняшний день молекулярно-генетические опухолевые биомаркеры, важно учесть результаты, которые играют ключевую роль в выборе стандартных терапевтических опций, а также выявить те, которые могут помочь найти альтернативные решения вне рамок стандартных режимов лечения, онкологи все чаще обращаются к комплексному геномному профилированию. Это исследование в общем понимании представляет собой использование расширенной таргетной NGS-панели для анализа ДНК опухоли. Также в 2024 году в рекомендации ESMO и NCCN было добавлено таргетное РНК секвенирование.
Выбор и использование таких диагностических инструментов должно определяться врачом-онкологом в каждом отдельном случае индивидуально с учетом истории лечения, типа опухоли, доступного биоматериала, доступных на рынке тестов.
Mosele MF, Westphalen CB, Stenzinger A, Barlesi F, Bayle A, Bièche I, Bonastre J, Castro E, Dienstmann R, Krämer A, Czarnecka AM, Meric-Bernstam F, Michiels S, Miller R, Normanno N, Reis-Filho J, Remon J, Robson M, Rouleau E, Scarpa A, Serrano C, Mateo J, André F. Recommendations for the use of next-generation sequencing (NGS) for patients with advanced cancer in 2024: a report from the ESMO Precision Medicine Working Group. Ann Oncol. 2024 Jul;35(7):588-606. doi: 10.1016/j.annonc.2024.04.005.
https://www.nccn.org/guidelines/category_1
https://www.rosoncoweb.ru/news/oncology/2024/05/29/
Сопроводительная терапия и реабилитация онкологических пациентов на различных этапах
Онкологическое лечение представляет собой сложный процесс, который часто приводит к радикальным изменениям в анатомических структурах организма (например, после хирургического вмешательства), оказывает системное воздействие на пациента (в случае химиотерапии) и вызывает лучевое поражение как опухолевых, так и нормальных тканей (при радиотерапии), что, в свою очередь, может негативно сказаться на функции органов и качестве жизни.
Среди наиболее распространенных изменений, которые можно и нужно предотвращать, выделяется нарушение нутритивного статуса пациента. Своевременное выявление снижения этого статуса и назначение лечебно-профилактических мероприятий, включая коррекцию диеты, помогают сохранить сил для продолжения лечения и поддерживают иммунный статус пациента и другие аспекты его здоровья.
Развитие нежелательных явлений на фоне химиотерапии, таргетной или иммунной терапии, таких как гастроэнтерологические расстройства, полинейропатия, дерматиты и другие, также может быть своевременно скорректировано, что позволит обеспечить непрерывность лечения при условии сохранения качества жизни пациента.
Пациенты часто сталкиваются с трудностями в повседневной деятельности, которые ограничивают возможность выполнения обычных рутин, не говоря уже о сохранении работоспособности и физической активности. Снижение качества жизни может стать причиной перерыва в лечении. Подобные ситуации необходимо предотвращать заранее. Например, в последние годы появляется все больше работ, которые говорят о важности физической активности для пациентов с таким диагнозом как рак поджелудочной железы. Они подчеркивают, что несмотря на агрессивное течение заболевания, поддержание функционального статуса, регулярные доступные физические упражнения ведут к изменению в иммунной системе и улучшают возможность получать химиотерапию.
Помимо желания предложить правильное, но сложное лечение, терапия должна сопровождаться намерением сохранить функциональный статус пациента и его жизненные силы на максимально возможном уровне. Тактика по сопроводительной терапии должна обсуждаться с лечащим доктором.
Chen L, Bai P, Kong X, Huang S, Wang Z, Wang X, Fang Y, Wang J. Prognostic Nutritional Index (PNI) in Patients With Breast Cancer Treated With Neoadjuvant Chemotherapy as a Useful Prognostic Indicator. Front Cell Dev Biol. 2021 Mar 30;9:656741. doi: 10.3389/fcell.2021.656741.
Mayer RS, Engle J. Rehabilitation of Individuals With Cancer. Ann Rehabil Med. 2022 Apr;46(2):60-70. doi: 10.5535/arm.22036.
Hsueh HY, Pita-Grisanti V, Gumpper-Fedus K, Lahooti A, Chavez-Tomar M, Schadler K, Cruz-Monserrate Z. A review of physical activity in pancreatic ductal adenocarcinoma: Epidemiology, intervention, animal models, and clinical trials. Pancreatology. 2022 Jan;22(1):98-111. doi: 10.1016/j.pan.2021.10.004.
Kurz E, Hirsch CA, Dalton T, Shadaloey SA, Khodadadi-Jamayran A, Miller G, Pareek S, Rajaei H, Mohindroo C, Baydogan S, Ngo-Huang A, Parker N, Katz MHG, Petzel M, Vucic E, McAllister F, Schadler K, Winograd R, Bar-Sagi D. Exercise-induced engagement of the IL-15/IL-15Rα axis promotes anti-tumor immunity in pancreatic cancer. Cancer Cell. 2022 Jul 11;40(7):720-737.e5. doi: 10.1016/j.ccell.2022.05.006.
“Мы развиваемся в рамках лучших практик персонализированной онкологии!”
В нашей практике мы стремимся соответствовать принципам персонализированной онкологии. Мы можем помочь пациенту в следующих вопросах
- разобраться с текущей тактикой лечения,
- определить и выполнить необходимые лабораторные, инструментальные исследования,
- определить и выполнить необходимые молекулярно-генетические исследования,
- уточнить следующие шаги в терапии,
- дать рекомендации по сопроводительной терапии в послеоперационном периоде и на фоне проводимой химиотерапии,
- определить объем реабилитации,
- определить тактику паллиативной помощи.